Anifrolumab—A Potential New Systemic Sclerosis Treatment
Redic M. et al. J. Clin. Med. 2026, 15, 1104. Review.
Introduction et contexte de l’étude
La sclérodermie systémique (ScS) est une maladie auto-immune rare caractérisée par une inflammation chronique, une altération du réseau microvasculaire et une fibrose de la peau et des organes.
Les interférons de type I (IFN-I), outre leur rôle dans la réponse antivirale, interviennent dans l’activation de l’immunité innée et adaptative ainsi que dans les maladies auto-immunes comme le lupus systémique. Chez les patients atteints de ScS, notamment ceux avec une forme diffuse cutanée et une atteinte des organes profonds, plusieurs études ont identifié une signature dite « interféron (IFN) » marquée par l’augmentation de l’expression de Gènes Stimulés par l’Interféron (« ISGs ») dans le sang et les tissus (peau et poumon).
In vitro, l’association entre IFN et fibrose a été clairement démontrée : l’activation par l’IFN des monocytes et des macrophages conduit à la sécrétion de médiateurs profibrotiques qui vont stimuler la prolifération des fibroblastes et leur synthèse de collagène.
Par ailleurs, l’activation chronique des cellules dendritiques par l’IFN-I favorise la transition fibroblaste-myofibroblaste via une signalisation IFN-α et CXCL4.
Dans les cellules endothéliales, les voies de signalisation inflammatoires induites par l’interféron de type 1 sont associées, entre autres, à une diminution de l’expression du facteur de transcription Fli-1, ce facteur étant essentiel à l’intégrité vasculaire. Un déséquilibre de l’expression de Fli-1, tout particulièrement sa diminution, peut induire des lésions vasculaires et favoriser aussi une fibrose.
L’IFN-I participe de plus à l’activation de la synthèse de TGF-β et au dépôt plus ou moins excessif de protéines de la matrice extracellulaire par les fibroblastes (ex : collagène) tandis que le TGF-β amplifie à la fois l’activation des récepteurs TLR et les voies de transcription induites par l’IFN dans ces cellules.
Ainsi, la signalisation de l’IFN-I favorise les dommages endothéliaux, l’inflammation périvasculaire et l’activation des fibroblastes, établissant une boucle auto-amplifiante de vasculopathie et de fibrose, deux caractéristiques qui définissent la ScS.
Méthode(s)
Cette revue étudie la littérature sur les données précliniques et cliniques évaluant le rôle de la voie de l’IFN-I dans la ScS et discute de l’intérêt thérapeutique potentiel de l’anifrolumab, un anticorps monoclonal entièrement humain ciblant la sous-unité 1 du récepteur de l’IFN-I (IFNAR1).
Résultat(s)
L’anifrolumab inhibe la signalisation de toutes les isoformes d’IFN-I, supprimant en aval l’activation de JAK–STAT et l’expression d’ISGs.
Dans les modèles murins de fibrose causée par la bléomycine, le blocage d’un régulateur clé de la signalisation de l’interféron de type I, l’interféron regulatory factor 7, entraîne une atténuation marquée de la fibrose dermique et de l’infiltration cellulaire inflammatoire.
Un essai clinique de phase 1 dans la ScS a démontré une suppression rapide de la signature IFN-I dans le sang et la peau après l’administration d’anifrolumab. Un essai clinique de phase III (DAISY NCT05925803) est en cours pour évaluer l’efficacité d’une injection sous-cutanée hebdomadaire d’anifrolumab dans la ScS pendant 52 semaines avec comme objectif primaire un critère composite
peau/poumon/qualité de vie/handicap (critère CRISS-25 révisé) (Table 1).
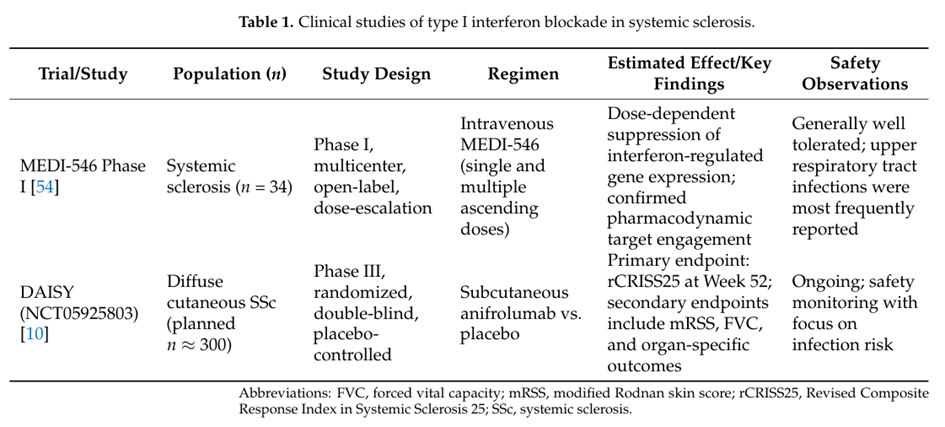
Figure issue intégralement de l’article.
Conclusion
Les essais cliniques actuels aideront à déterminer l’efficacité, la sécurité et le profil des patients qui pourront bénéficier de l’anifrolumab : ceux ayant une signature IFN-I élevée ? les formes inflammatoires cutanées précoces ?
Toutefois, il ne faudra pas négliger le risque d’infection, en particulier de la réactivation du zona, sous traitement par anifrolumab.
Message(s) clé
– A l’instar du lupus, des arguments physiopathologiques soutiennent la justification du ciblage thérapeutique de la voie IFN-I au cours de la ScS.
– Au sein des biothérapies utilisées dans la ScS, l’anifrolumab occupe une position unique en ciblant l’axe IFN-I, un régulateur central de l’immunité, l’intégrité vasculaire et fibrotique.
– Les résultats de l’essai DAISY nous permettront de mieux apprécier son potentiel thérapeutique dans la forme cutanée diffuse de patients souffrant de ScS.
Référence Pubmed: Radić M, PrižmićPS, Bečić T, et al. Anifrolumab-A Potential New Systemic Sclerosis Treatment. J Clin Med 2026 Jan 30;15(3):1104.
